Macrophages de type M1, Phénotypage et/ou Libération de cytokines (stimulation IFN- gamma + LPS)
MONO-0007- Contexte
- Description
- Prérequis
- Etude et rapport
- Voir également
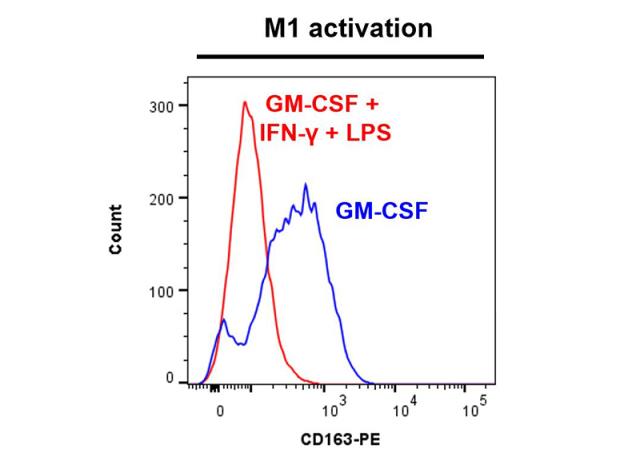
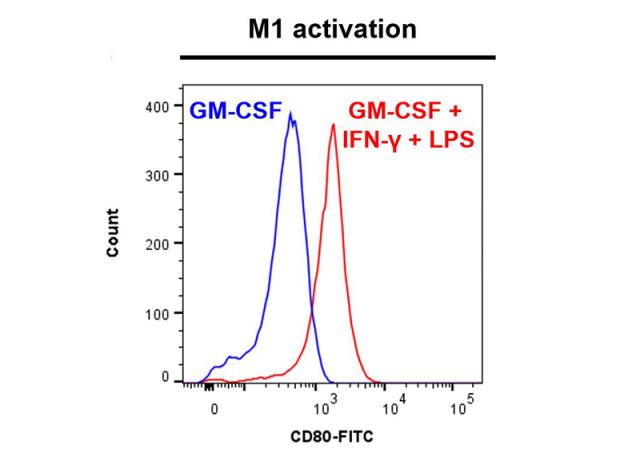
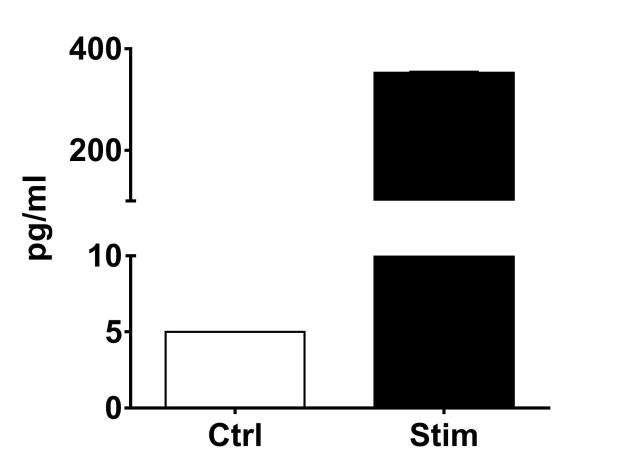
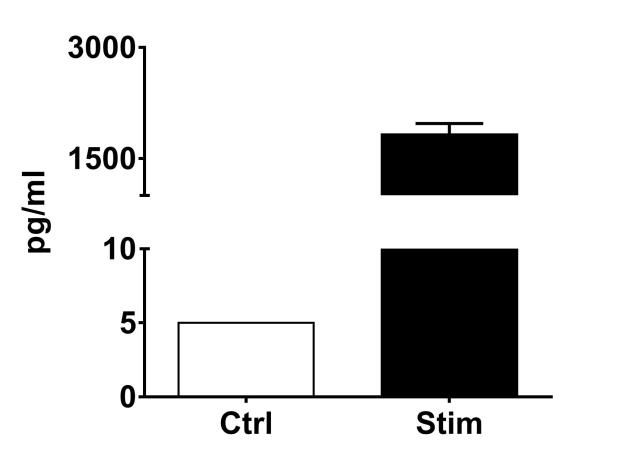
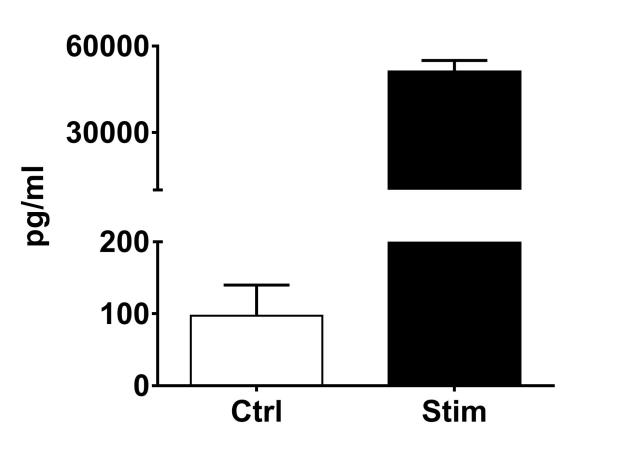
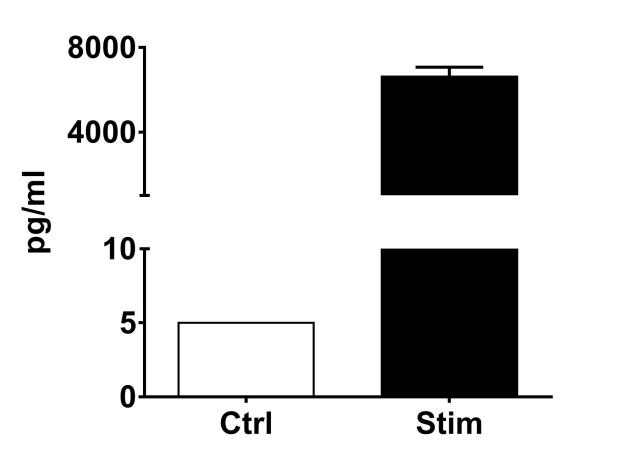
Les monocytes et les macrophages constituent les premiers éléments de défense contre des agents étrangers et participent à la régulation de la réponse immunitaire adaptative. Les monocytes circulants pénètrent les tissus périphériques lésés ou inflammés au sein desquels ils vont se différencier en différents types de macrophages résidents. De la même manière que les cellules T helper (Th), les macrophages sont classifiés en 2 catégories: les macrophages de type 1, classiquement activé (M1) et les macrophages de type 2, activés dans des contextes plus spécifiques. Les macrophages M1 sont caractérisés par un phénotype pro-inflammatoire ainsi qu’une activité anti-microbienne, alors que les macrophages de type M2 sont impliqués dans des processus d’angiogenèse, de réparation ou encore de remodelage de la matrice. Le principe de ce test in vitro réalisé sur des macrophages M1 activés par une stimulation IFNg+LPS consiste à mesurer par cytométrie en flux la capacité de composés à moduler la libération de cytokines pro-inflammatoires (TNF-alpha, IL-1beta, IL-6, IL-10 et/ou IL12p70) et/ou à moduler le niveau d’expression des marqueurs CD80 et CD163, respectivement décrit comme des marqueurs de polarité M1 et de polarité M2.
| Modèle biologique | Macrophages dérivés de monocytes (CD14+) et polarisés M1 (traitement GM-CSF) |
|---|---|
| Espèce | Humain |
| EndPoint | Libération de TNF- alpha, IL1 beta, IL-6, IL-10, IL12p70 |
| Méthode | Cytométrie en flux (multiplexe) |
| Facteur de stimulation | IFN- gamma (100 ng/ml) + LPS (1 ng/ml) |
| Composé de référence | Dexaméthasone |
| Physiopathologie | Système sanguin, lymphatique, appareil cardiovasculaire et immunité > Tests d'immuno-inflammation sur sang/cellules immunitaires > Monocytes/macrophages |
Quantité requise de composés : généralement quelques mg ou ml, la quantité requise est fonction de la forme et solubilité de vos composés et des concentrations à l’essai. Contactez-nous pour toute estimation.
Initiation des essais et délais : l’initiation des essais est assujettie à la réception de votre bon accord et de vos composés à l’essai. La date d’envoi du rapport d’étude vous est communiquée par email lors du démarrage de l’étude. Avec 5 à 10 semaines en moyenne nos délais peuvent être soumis à certaines fluctuations (disponibilité des échantillons biologiques, plan de charge…).
Prix : notre tarification fonctionne sur une base d’étude forfaitaire + tarification à l’unité (prix au point ou à la condition expérimentale).
Proposition d’étude, faisabilité :
Notre équipe commerciale est à votre écoute :
Protocoles à façon : comme tous nos tests, celui-çi peut faire l’objet d’un protocole adapté à vos besoins. Pour toute question contactez-nous !
Initiation des essais et délais : l’initiation des essais est assujettie à la réception de votre bon accord et de vos composés à l’essai. La date d’envoi du rapport d’étude vous est communiquée par email lors du démarrage de l’étude. Avec 5 à 10 semaines en moyenne nos délais peuvent être soumis à certaines fluctuations (disponibilité des échantillons biologiques, plan de charge…).
Prix : notre tarification fonctionne sur une base d’étude forfaitaire + tarification à l’unité (prix au point ou à la condition expérimentale).
Proposition d’étude, faisabilité :
Notre équipe commerciale est à votre écoute :
- Etude de la faisabilité technique de votre projet
- Stratégie de sélection de tests
- Définition du plan d’expérience
- Estimation financière et accords contractuels (coûts, délais, contrats de confidentialité…)
Protocoles à façon : comme tous nos tests, celui-çi peut faire l’objet d’un protocole adapté à vos besoins. Pour toute question contactez-nous !
Direction d’étude : parce que chaque projet nécessite conseils et expertise, toute étude est pilotée et contrôlée par un directeur d’étude attitré et à votre écoute.
Validation : les tests présentés au catalogue ont fait l’objet d’une validation préliminaire et sont soumis à des procédures opérationnelles standard (SOPs) ainsi qu’à des critères de validation. Cependant, selon les modèles et méthodes analytiques, la robustesse peut être différente d'un test à l'autre , n'hésitez pas nous contacter pour plus de précisions.
Rapport et données expérimentales : nos prestations comprennent l’édition d’un rapport d’étude synthétique et scientifique, rédigé en anglais ou en français, au format PDF ou Microsoft® Office.
Laboratoire / Lieu : comme tous nos tests, ce test est réalisé dans notre laboratoire à Gençay (France).
Validation : les tests présentés au catalogue ont fait l’objet d’une validation préliminaire et sont soumis à des procédures opérationnelles standard (SOPs) ainsi qu’à des critères de validation. Cependant, selon les modèles et méthodes analytiques, la robustesse peut être différente d'un test à l'autre , n'hésitez pas nous contacter pour plus de précisions.
Rapport et données expérimentales : nos prestations comprennent l’édition d’un rapport d’étude synthétique et scientifique, rédigé en anglais ou en français, au format PDF ou Microsoft® Office.
Laboratoire / Lieu : comme tous nos tests, ce test est réalisé dans notre laboratoire à Gençay (France).
| Référence | Titre | EndPoint | Méthode |
|---|---|---|---|
| Référence | Titre | EndPoint | Méthode |
| PBMC-0046 | PBMC, libération de cytokines (stimulation TNF- alpha) | *** (authentification requise) | *** (authentification requise) |
| PBMC-0045 | PBMC, libération de cytokines (stimulation extrait de kératinocytes) | *** (authentification requise) | *** (authentification requise) |
| PBMC-0044 | PBMC, libération de cytokines (stimulation IL-1 alpha) | *** (authentification requise) | *** (authentification requise) |
| CD19BL-0005 | LB CD19+, phénotypage & prolifération (basal) | Prolifération | Cytométrie en flux Incorporation de [3H]-thymidine |
| MONO-0015 | Monocytes CD14+, Libération de cytokines (basal) | *** (authentification requise) | *** (authentification requise) |
| PBMC-0042 | PBMC, Induction de macrophages de type M2 dans une culture RLM (Réaction Lymphocytaire Mixte) (basal) | *** (authentification requise) | *** (authentification requise) |
| PBMC_Lb-0002 | PBMC, libération de métabolites de l'acide arachidonique (stimulation au A23187) | *** (authentification requise) | *** (authentification requise) |
| PBMC_Lb-0001 | PBMC, libération de PGE2 (stimulation LPS) | *** (authentification requise) | *** (authentification requise) |
| THP1-0007 | THP-1, libération d'IL-1 beta (stimulation LPS) | *** (authentification requise) | *** (authentification requise) |
| MONO-0004 | Monocytes, marquage de récepteurs opïoides (Basal) | Expression de ChemR23 Expression de GPR120 Expression du récepteur aux opioïdes de type delta 1 (OPRD1) Expression du récepteur opiacé delta (DOR) Expression du récepteur opiacé mu (MOR) | Cytométrie en flux |